EXTRACCION
La extracción es la técnica empleada para separar un producto orgánico de una mezcla de reacción o para aislarlo de sus fuentes naturales. Puede definirse como la separación de un componente de una mezcla por medio de un disolvente.
En la práctica es muy utilizada para separar compuestos orgánicos de las soluciones o suspensiones acuosas en las que se encuentran. El procedimiento consiste en agitarlas con un disolvente orgánico inmiscible con el agua y dejar separar ambas capas. Los distintos solutos presentes se distribuyen entre las fases acuosas y orgánica, de acuerdo con sus solubilidades relativas.
De este modo, las sales inorgánicas, prácticamente insolubles en los disolventes orgánicos más comunes, permanecerán en la fase acuosa, mientras que los compuestos orgánicos que no forman puentes de hidrógeno, insolubles en agua, se encontrarán en la orgánica.
Equipo y procedimiento
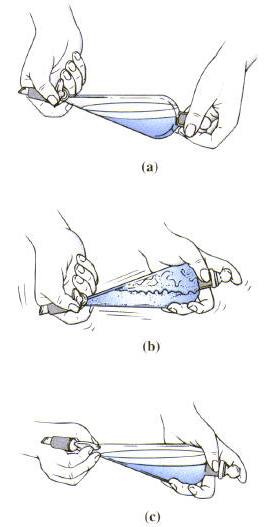
El aparato utilizado en las extracciones es el embudo de separación que se muestra en la figura. El tapón y la llave, que deben estar bien ajustados, se lubrican con una grasa adecuada antes de cada uso.
El embudo de decantación debe manejarse con ambas manos; con una se sujeta el tapón -asegurándolo con el dedo índice- y con la otra se manipula la llave. Se invierte el embudo y se abre la llave para eliminar la presión de su interior; se agita con suavidad durante uno o dos segundos y se abre de nuevo la llave.
Después de separadas ambas fases, se saca el inferior por la llave y la superior por la boca; así se previenen posibles contaminaciones. El número de extracciones necesarias en cada caso particular depende del coeficiente de reparto y de los volúmenes relativos de agua y de disolvente. La posición relativa de las capas acuosa y orgánica depende de sus densidades. En caso de duda puede determinarse la identidad de cada una de ellas ensayando la solubilidad en agua de unas gotas de la misma. Es una medida prudente, en especial cuando se trata de reacciones nuevas, conservar todos los extractos y líquidos residuales hasta comprobar que se obtiene el producto final con el rendimiento esperado; sólo entonces debe procederse a la limpieza.
Emulsiones
Con frecuencia, sobre todo cuando se trabaja con soluciones alcalinas, se forman emulsiones durante el proceso de extracción. Estas pueden romperse, de ordinario, mediante:
1) un movimiento de giro suave al líquido del embudo de separación, mantenido en su posición normal;
2) agitación vigorosa de la capa emulsionada con una varilla de vidrio;
3) saturación de la capa acuosa con sal común;
4) centrifugación.
El método 3, de saturación con sal, tiene una doble ventaja: hace disminuir la solubilidad en agua de la mayor parte de los solutos y de los disolventes orgánicos. Su nombre es efecto salino.
Extracción con bases
Con frecuencia se consiguen separaciones muy netas de compuestos orgánicos, utilizando soluciones ácidas o alcalinas capaces de convertir dichas sustancias en sales, solubles en agua e insolubles en éter.
Purificación de ácidos y fenoles
Una solución de hidróxido sódico al 5-10 % convierte, por ejemplo, los ácidos carboxílicos, R-COOH, en sus sales sódicas, R-COO-, Na+. Los compuestos fenólicos experimentan una transformación semejante con el mismo reactivo. Por esta causa puede utilizarse una solución de hidróxido sódico para extraer un ácido carboxílico o un compuesto fenólico de su solución en un disolvente orgánico o, recíprocamente, liberar estos tipos de compuestos de sus impurezas orgánicas por extracción de sus soluciones alcalinas con un disolvente adecuado.
Separación de ácidos y fenoles
Las soluciones acuosas de bicarbonato sódico convierten también los ácidos carboxílicos en sus respectivas sales sódicas, pero no son lo suficientemente básicas para formar sales con los compuestos fenólicos. Esta es la base de un elegante método de separación de ácidos carboxílicos y fenoles: el ácido se extrae en primer lugar de su solución en un disolvente orgánico con una solución de bicarbonato sódico y, posteriormente, el fenol con solución de sosa.
Los ácidos inorgánicos se eliminan con facilidad de los disolventes orgánicos por extracción con una solución de hidróxido, carbonato o bicarbonato sódicos.
Extracción con ácidos
El ácido clorhídrico diluido se emplea con frecuencia para la extracción de sustancias básicas de sus mezclas con otras neutras o ácidas, o bien para eliminar impurezas básicas. El ácido diluido convierte la base, p.ej., amoniaco o una amina orgánica (R3N), en el correspondiente hidrocloruro (R3NH+Cl-), soluble en agua. Por otra parte, las impurezas orgánicas que acompañan a una amina pueden eliminarse por extracción de las mismas con un disolvente orgánico de una solución ácida de aquella.
Las sales sódicas de los ácidos carboxílicos y de los fenoles son fácilmente convertibles en los compuestos de partida por tratamiento de ácido sulfúrico o fosfórico. Los hidrocloruros de las aminas se transforman de nuevo en éstas por adición de una solución de hidróxido sódico.
APLICACIONES
La implantación de la operación de extracción líquido-líquido a gran escala en procesos industriales fue más tardía que el resto de operaciones, destilación y absorción. Sin embargo la importancia del proceso de extracción líquido-líquido ha ido en aumento debido a la creciente demanda de productos sensibles a la temperatura, mayores requerimientos de pureza, equipos más eficientes y la disponibilidad de disolventes más selectivos.
Por otro lado, se suele preferir la aplicación del proceso de extracción a la destilación en los siguientes casos:
- si existen sustancias inorgánicas complejas disueltas en soluciones orgánicas o acuosas
- si es preciso retener un componente que se encuentra en una concentración muy pequeña
- en la recuperación de sustancias sensibles a la temperatura
- si la separación se basa más en la naturaleza de las sustancias que en su distinta volatilidad
- si la mezcla posee puntos de ebullición o de fusión muy próximos
- si la mezcla presenta azeótropos
La extracción líquido-líquido presenta una amplia aplicación en la industria del petróleo para separar alimentaciones líquidas en función de su naturaleza química más que por su peso molecular o la diferencia de volatilidad. Como ejemplo se tiene la separación entre hidrocarburos aromáticos, alifáticos y nafténicos.
Otras aplicaciones se pueden encontrar en:
la industria bioquímica como la separación de antibióticos y la recuperación de proteínas de sustratos naturales.

- la extracción de metales como la recuperación del cobre de soluciones amoniacales y separaciones de metales poco usuales y de isótopos radiactivos en elementos combustibles gastados.
- la industria química inorgánica para recuperar compuestos tales como ácido fosfórico, ácido bórico e hidróxido de sodio de soluciones acuosas.
- recuperación de compuestos aromáticos como fenol, anilina o compuestos nitrogenados de las aguas de desecho, ya que constituyen una fuente contaminante.
- recuperación de productos sensibles al calor
- recuperación de compuestos orgánicos del agua como formaldehido, ácido fórmico y ácido acético.
AVANCES TEGNOLOGICOS
Recientes avances tecnológicos posibilitan hoy la extracción de mayores cantidades de crudo de viejos yacimientos. Al mismo tiempo, el alza de precios hizo más costeable la búsqueda de reservas difíciles de alcanzar. Así, las predicciones fatalistas sobre el fin de reservas mundiales dan paso a nuevos pronósticos que indican la existencia de más crudo.
Durante la década pasada, los avances tecnológicos posibilitaron la extracción de mayores cantidades de petróleo de los viejos yacimientos y, al mismo tiempo, el alza de precios hizo más costeable para las compañías la búsqueda de reservas difíciles de alcanzar. Al saber que aún hay mucho petróleo en los yacimientos conocidos, las predicciones fatalistas que señalan el fin de las reservas mundiales dan paso a nuevos pronósticos los cuales indican que podremos encontrar más crudo que antes.
Aún existe una perspectiva minoritaria –apoyada sobre todo por un pequeño grupo de geólogos petroleros jubilados y algunos miembros del Congreso estadounidense–, quienes sostienen que la producción petrolera ya alcanzó su nivel más alto, pero esa teoría se desploma. Igual de polémica es para las compañías petroleras la opinión, cada vez más extendida, de los ambientalistas, quienes rechazan la extracción y el consumo de cantidades cada vez mayores de combustible fósil.



